“A terapia celular não é apenas uma nova esperança para o tratamento do cancro, na medida em que ela já é uma realidade dos nossos dias. A questão é que gostávamos que, no futuro, essa realidade fosse o mais transformadora possível.” Quem o diz, de modo tão otimista, é Bruno Silva-Santos, investigador e, desde 2014, vice-diretor do Instituto de Medicina Molecular (IMM), em Lisboa, um dos especialistas que – juntamente com Cláudia Delgado, diretora médica da Gilead, e Maria Gomes da Silva, diretora do Serviço de Hematologia do Instituto Português de Oncologia (IPO) de Lisboa – participaram no mais recente Conversas com Saúde, organizado pela VISÃO em parceria com a Gilead.
A linguagem bélica pode ajudar a explicar do que falamos quando falamos em terapia celular uma vez que as células são como que “armadas” para a “batalha” contra o cancro. A palavra, novamente, a Bruno Silva-Santos: “A terapia celular é o uso de células imunitárias, isto é, glóbulos brancos que se encontram no nosso sangue e que tipicamente respondem a agentes infeciosos (estão na base, por exemplo, das vacinas que temos para a Covid-19), mas que também respondem a cancro. O que fazemos é usar essa capacidade destas células imunitárias para matar células tumorais e, assim, definir uma imunoterapia para o cancro”.
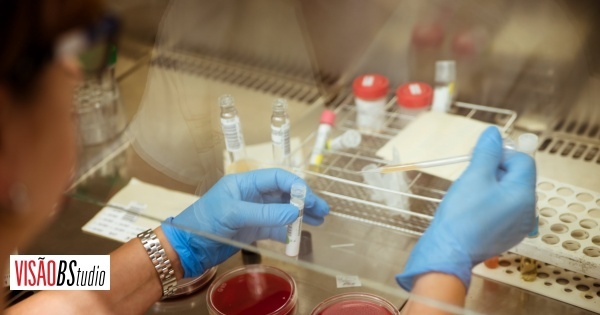
As células imunitárias são manipuladas no laboratório de forma a receberem um recetor que, depois, lhes vai permitir detetar a célula que queremos eliminar, neste caso, a que está na base do cancro hematológico do doente
Bruno silva-santos, vice-diretor do Instituto de Medicina Molecular
A terapia celular está aprovada nos Estados Unidos da América desde 2017 e, na Europa, desde 2018. Em Portugal, os primeiros passos na sua utilização em doentes oncológicos foram dados logo no ano seguinte, em 2019, no Instituto Português de Oncologia de Lisboa e no do Porto. Mais recentemente, também o Hospital de Santa Maria aderiu à terapêutica que, por enquanto, apenas pode ser usada em linfomas, leucemia aguda e mieloma múltiplo. As células CAR-T são uma terapia celular dirigida, explica ainda o investigador do IMM, ou seja, personalizada para cada doente. “As tais células imunitárias são manipuladas no laboratório de forma a receberem um recetor (isto é, uma proteína especial que está na superfície destas células) que, depois, lhes vai permitir detetar a célula que queremos eliminar, neste caso, a célula que está na base do cancro hematológico do doente”, continua.
Uma luta contra o tempo
No Instituto Português de Oncologia de Lisboa, Maria Gomes da Silva revela a sua experiência com a terapia celular. Em constante comunicação com outros profissionais de saúde que, em Portugal e na Europa, têm estado a lidar o mesmo tratamento, a médica tem já, conforme relata, alguma noção do que podem ser as dificuldades na sua utilização. Segundo os seus cálculos, em Portugal, já devem ter beneficiado desta terapia um pouco mais de 40 doentes oncológicos. É sempre uma luta contra o tempo uma vez passa cerca de um mês entre o momento da colheita, o momento em que as células são manipuladas em laboratório e, depois, são infundidas no doente. E, por vezes, como nota a diretora do Serviço de Hematologia do IPO de Lisboa, “não é simples fazer os doentes esperar um mês”. “É uma obra de arte logística, e é uma luta minuto a minuto”, afirma. E acrescenta: “Não há doentes certos, há doentes que precisam. Mas, entre todos os doentes que precisam, há aqueles que nós sabemos que têm mais hipóteses de beneficiar desta terapêutica”.
O nosso contributo foi gerar toda uma robustez de evidência, através dos ensaios clínicos que foram sendo feitos com várias populações de doentes
Cláudia delgado, diretora médica da gilead
Em breve, quando a fábrica da Gilead na Holanda, que por enquanto funciona apenas como uma primeira paragem até ao destino final das células colhidas, nos Estados Unidos da América, puder assegurar todo o processo, vai ser possível reduzir o tempo de espera, diz Cláudia Delgado. “O nosso contributo foi gerar toda uma robustez de evidência, através dos ensaios clínicos que foram sendo feitos com várias populações de doentes. Mas também é muito importante que as pessoas percebam que existe segurança. A terapia celular representa um grande avanço da Ciência, mas também existe um conjunto de produção de evidência e de aprovação pelas entidades reguladoras [que garante a segurança]”, sustenta a diretora médica da Gilead.
As complicações gravíssimas, e eventualmente mortais, desta terapêutica, que evidentemente existem, são muito raras
maria gomes da silva, diretora do serviço de hematologia do instituto português de oncologia de lisboa
Sobre os eventuais efeitos adversos da terapia celular, Cláudia Delgado acrescenta que estes se colocam, sobretudo, ao nível neurológico. Da sua experiência, salienta Maria Gomes da Silva que, de um modo geral, os médicos têm conseguido reprimir as complicações, também por causa do cuidado e no rigor que colocam na seleção dos doentes a submeter ao tratamento. “As complicações gravíssimas, e eventualmente mortais, desta terapêutica, que evidentemente existem, são muito raras. Já as complicações graves não são raras, mas, na esmagadora maioria dos doentes, nós conseguimos manejar as toxicidades sérias, que são relativamente precoces”, diz a médica do IPO.
No futuro, é expectável que a terapia celular possa também vir a ser utilizada noutro tipo de cancros. Mais uma vez, cabe a Bruno Silva-Santos dar uma nota de otimismo: “A década passada foi a década da imunoterapia do cancro, na vertente da terapia celular e também na vertente dos chamados inibidores de checkpoints (mais usados nos cancros sólidos). Agora, nesta nova década, temos de construir e criar mais novidade que vai beneficiar doentes que, neste momento, ainda não têm a imunoterapia como solução”.
Para ouvir em Podcast: