“Benefícios”, “riscos”, “segurança” foram das palavras mais usadas nas perguntas feitas por várias pessoas em representação de outras tantas entidades da União Europeia (UE) durante uma sessão pública online sobre vacinas contra a Covid-19, que a Agência Europeia de Medicamentos (EMA, na sigla em inglês) organizou, esta sexta-feira, para dar a conhecer os processos de desenvolvimento, avaliação, aprovação e monitorização destas vacinas, bem como o papel da EMA nas várias fases.
Na primeira parte da sessão com o tema “How safe and effective vacines are developed and authorised in the EU” (“De que forma as vacinas desenvolvidas e autorizadas na União Europeia são eficazes e seguras”), moderada por Noël Wathion, vice-diretor executivo da EMA, quatro especialistas explicaram como se desenvolve um vacina, desde o zero, todos os estudos que são feitos e a forma como são feitos até se chegar à fase de ensaios clínicos em humanos que se desenrola em três fases. Foi esclarecido que as vacinas passaram por todas as fases que estão delineadas para qualquer outra vacina, só que, desta vez, dada a urgência, o tempo foi “muito comprimido”, como destacou Marco Cavalleri, da agência, embora todos os “critérios tenham sido rigorosamente cumpridos”. “Isto só foi possível [ter vacina prontas para aprovação tão depressa] porque foram disponibilizados meios para isso”, notou.
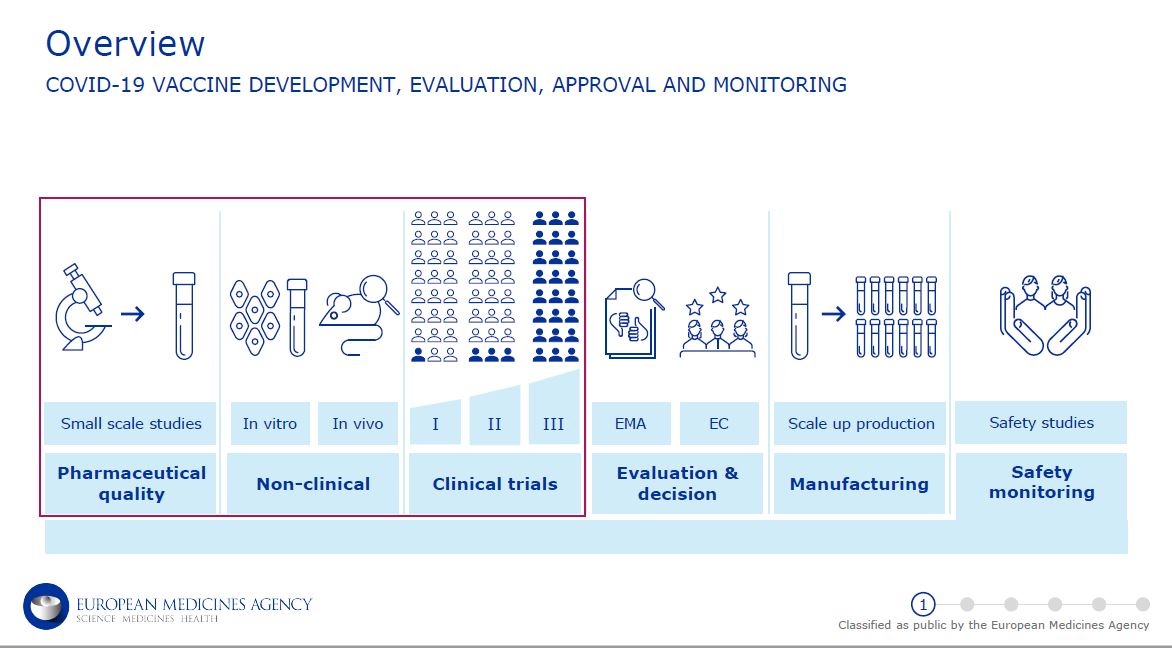
Foto: Captura de escrã
No evento, apresentou-se como vai ser feita a monitorização das vacinas, para que sejam “tomadas medidas rapidamente sempre que necessário”, disse Peter Arlett, também da EMA, que recordou que “nenhum medicamento é 100% seguro, então, como qualquer outro medicamento, as vacinas podem ter efeitos secundários”. “A maioria é leve, ou mesmo rara, e os efeitos secundários graves devem ser balanceados com a prevenção de doenças graves ou mesmo fatais como a Covid-19”, acrescentou, lembrando o custo/benefício das vacinas.
A especialista em comunicação referiu que, mais do que nunca, as pessoas precisam de ter “acesso aos dados” para perceberem a “importância das decisões que se tomam sobre as vacinas”, além de que a “transparência” é essencial em todo o processo e “requer um esforço extra na comunicação”.
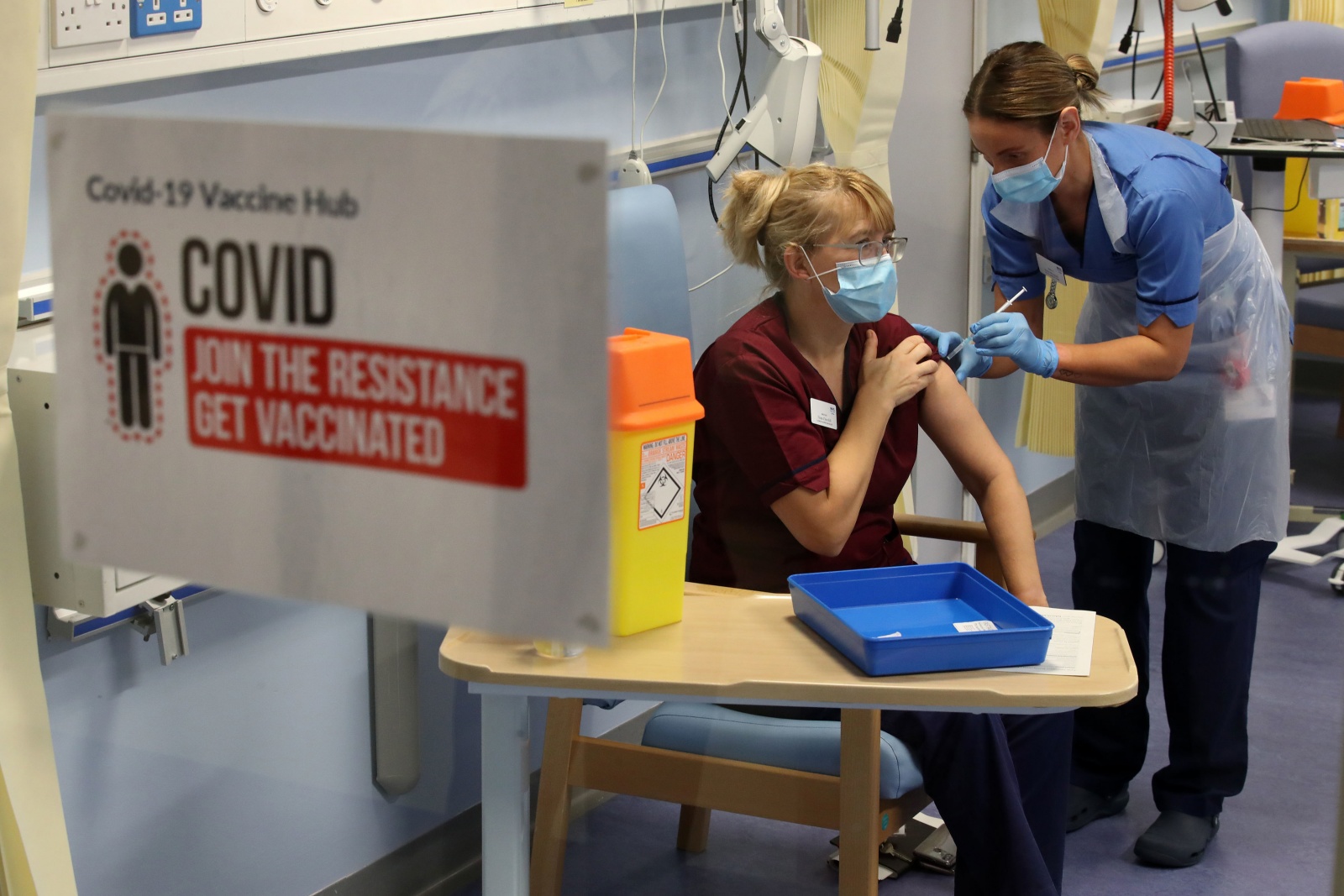
Foto: Getty Images
Na segunda parte da sessão, que teve a duração total de três horas e meia, intervieram 15 pessoas de vários setores, tanto da academia, como da Saúde, ou de instituições da UE ligadas à Hematologia, Coração ou Doenças Raras, por exemplo. No ar foram deixadas algumas afirmações: “A vacina não acaba com a pandemia, a vacinação é que o pode fazer”; “Os benefícios e os riscos das vacinas devem ser melhor explicados”. Mas, sobretudo, foram deixadas muitas perguntas: “Quem já teve Covid-19 deve receber a vacina?”; “Qual a duração da imunidade das vacinas?”; “As pessoas com doenças raras não deviam ser prioritárias na vacinação?”; “Quais são os efeitos por serem utilizadas em diferentes populações e idades”; “Qual o comportamento das vacinas nas pessoas com a imunidade deprimida?”
Também foram lançados apelos. Para que os Governos peçam “a colaboração dos farmacêuticos no processo de vacinação massiva”, disse Tjalling van der Schors, da Associação Europeia dos Farmacêuticos Hospitalares, porque, “além de haver vacinas diferentes” que se podem adaptar melhor a cada pessoa, estes profissionais também podem “ter um papel importante na deteção de pessoas pertencentes a grupos de risco”. Outra solicitação veio de Nikolas Dietis, da Universidade do Chipre, para que todos os dados sobre o desenvolvimento e fabrico das vacinas sejam públicos e não “apenas as informações que as empresas publicam”.







































































