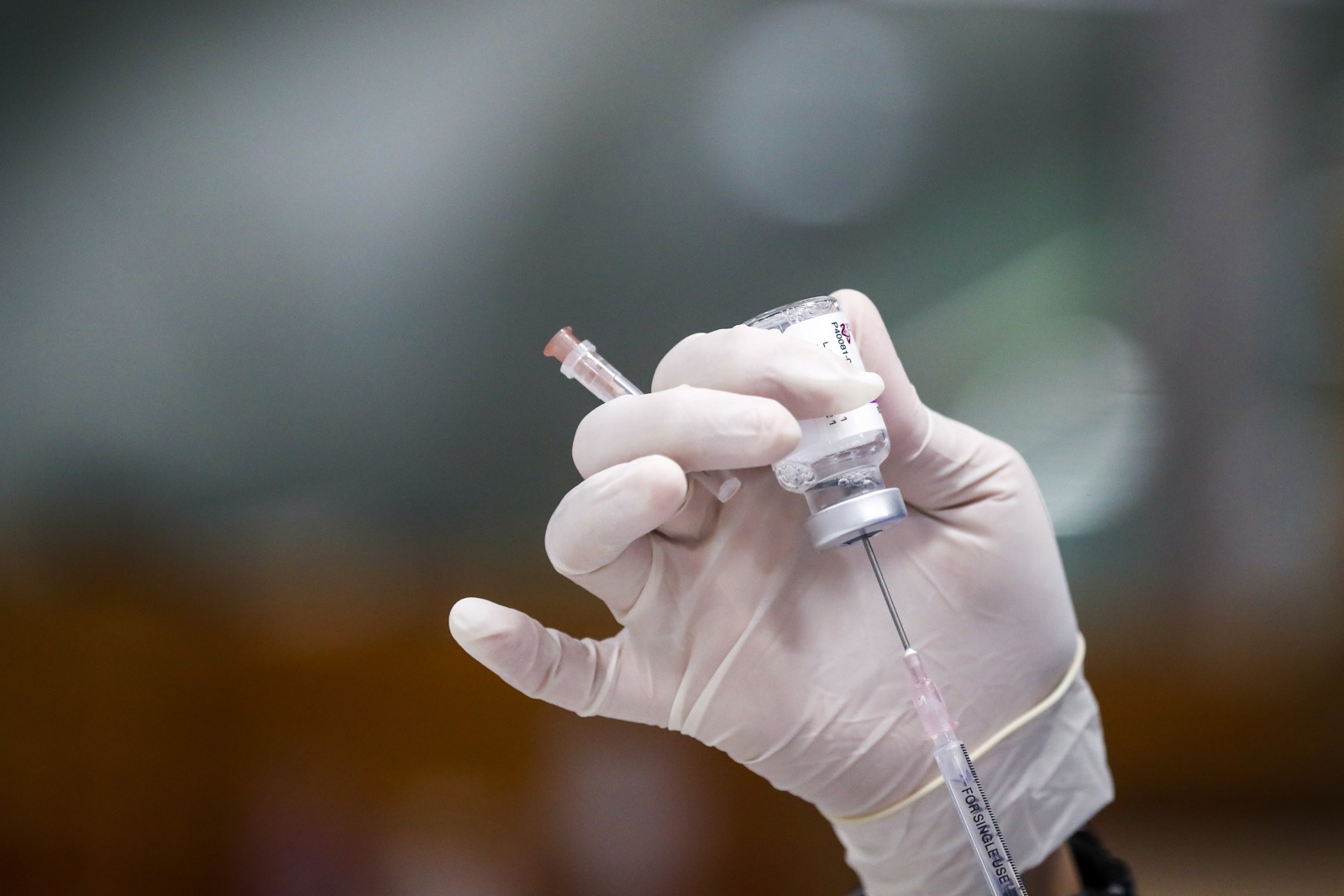
Atualmente, através da Comissão Europeia, Portugal tem seis vacinas contratualizadas e outras duas em fase de discussão. A diretora da Unidade de Avaliação Científica do Infarmed, Fátima Ventura, debruçou-se sobre a evolução da investigação ao nível das vacinas contra a Covid-19 na reunião que voltou a reunir representantes políticos e especialistas em saúde pública nas instalações da autoridade do medicamento, em Lisboa.
Neste momento, estão 30 vacinas na fase III dos ensaios clínicos e oito em fase IV, o que significa que estas últimas já foram aprovadas, mas continuam a ser investigadas.
De acordo com a especialista, estão planeados ensaios clínicos com a vacina Comirnaty (Pfizer-BioNTech) dos zero aos seis meses e dos seis meses aos 12 anos. No caso da Spikevax (Moderna) e da Vaxzevria (AstraZeneca) os testes serão realizados dos zero aos 12 anos e no da Janssen (Johnson & Johnson) dos zero aos 18 anos. Todas as vacinas já aprovadas têm planeados ensaios clínicos com imunodeprimidos.
Fátima Ventura sublinhou que várias alterações de fabrico permitiram aumentar a capacidade de produção de vacinas, também a extensão do prazo de validade dos fármacos contribuiu para uma maior flexibilidade dos planos de vacinação.
Aguardam-se, “ansiosamente”, novas posologias, ao nível de doses de reforço ou adicionais das vacinas. A especialista fez questão de esclarecer a diferença entre ambas: “A dose de reforço é administrada a pessoas que completaram o esquema de vacinação primário e tem como objetivo restaurar a proteção”.
Já a dose adicional é dirigida a pessoas com o sistema imunitário comprometido, “que não responderam de todo ou não responderam adequadamente ao esquema de vacinação prévio”.
Atualmente, a Agência Europeia do Medicamento (EMA) está a avaliar o pedido de autorização para a administração de uma dose de reforço da Comirnaty (Pfizer-BioNTech) à população em geral. Se for aprovada, a terceira dose deverá ser inoculada seis meses após a segunda injeção, aos maiores de 16 anos. A decisão da EMA deverá ser conhecida dentro de semanas (prevê-se que também a Spikevax (Moderna) e a Janssen façam pedidos de aprovação semelhantes).
Ao mesmo tempo, a EMA também está a analisar a administração de doses adicionais (a pessoas imunodeprimidas) da Pfizer-BioNTech e da Moderna.
O Centro Europeu de Prevenção e Controlo das Doenças (ECDC) e a EMA publicaram uma posição conjunta na qual defendem que não é urgente a inoculação de doses de reforço, à luz da evidência existente, e defendem que a prioridade deve ser vacinar aqueles que ainda não estão imunizados. Até agora, os dados disponíveis indicam que as vacinas continuam a garantir uma elevava proteção contra hospitalização, doença grave e morte. No entanto, a definição dos planos de vacinação é da responsabilidade dos Estados nacionais.
Fátima Ventura destacou que, segundo as autoridades europeias, a efetividade da vacina contra doença grave deve ser o indicador charneira para avaliar a necessidade de doses de reforço. “Ainda é preciso perceber se há uma correlação entre a proteção e os anticorpos, qual o intervalo ótimo entre a segunda dose e a dose de reforço, ter em consideração as variantes e esquemas vacinais homólogos [com a mesma vacina] ou heterólogos [com vacinas diferentes]”, notou, lembrando que só mais estudos dar resposta a estas questões.
Contudo, a EMA reconhece que podem já começar a ser administradas doses adicionais em indivíduos imunocomprometidos e em idosos mais frágeis, tal como já acontece em Portugal.
A representante do Infarmed levantou a questão sobre se será necessário adaptar as vacinas às novas variantes em circulação. Tanto a EMA como as farmacêuticas acreditam que sim, mas para tal é necessário monitorizar a efetividade da vacina. Ao mesmo tempo, a experiência com a vacina da gripe indica que não serão necessários ensaios clínicos muito complexos para fazer esta adaptação às novas variantes.
Alguns dos contratos já celebrados com as farmacêuticas preveem o fornecimento destas vacinas adaptadas, mas ainda não foram submetidos pedidos de autorização para a sua introdução no mercado. A Moderna está a desenvolver uma vacina multivalente (que mistura a vacina aprovada com outra contra a variante Beta), que poderá ser apresentada em breve e também um fármaco direcionado para a Delta.
Entre as vacinas ainda em avaliação, que ainda não apresentaram pedidos para entrar no mercado, estão a Novavax e a Sanofi e, também, a Curevac, todas elas contratualizadas com a União Europeia.